
Physique et Chimie : 2ème Bac SPC
Semestre 1 Devoir 3 Modèle 1
Professeur : Mr El GOUFIFA Jihad
Exercice 1 (7 pts)
Les condensateurs sont caractérisés par le fait d’emmagasiner de l’énergie électrique pour l’utiliser au cas de besoin. Cette propriété permet d’utiliser les condensateurs dans beaucoup d’appareils.
On réalise le montage de la figure 1 formé de :
- Un générateur idéal du courant qui alimente le circuit par un courant d’intensité .
- Un condensateur de capacité initialement déchargé.
- Un conducteur ohmique de résistance .
- Un interrupteur à deux positions et .
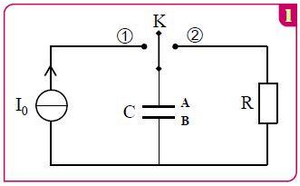
A on bascule l’interrupteur à la position et on suit les variations de la tension en fonction du temps et on obtient la courbe de la figure 2 :
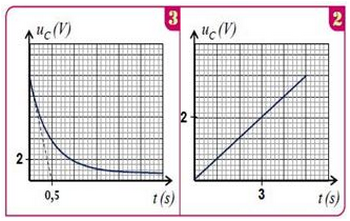
- Déterminer l’armature négative.
- Montrer que l’expression de la tension aux bornes du condensateur s’écrit : .
- Vérifie que .
Lorsque la tension aux bornes du condensateur est égale à , on bascule l’interrupteur à la position et on obtient la courbe de la figure 3 ci-dessus.
On considère que
- Déterminer l’équation différentielle vérifié par .
- Vérifier que est solution de l’équation différentielle
- Par l’analyse dimensionnelle montrer que a une dimension du temps.
- Déterminer la valeur de et déduire la valeur de la résistance
- Montrer que l’expression de l’intensité du courant est :
- Déterminer à l’instant où de l’énergie maximale stockée dans le condensateur est dissipée par effet joule.
Exercice 2 (6 pts)
Pour étudier expérimentalement la réponse d’un dipôle à un échelon de tension, on réalise un circuit électrique en associant en série :
- Une bobine d’inductance et de résistance .
- Un résistor de résistance .
- Un générateur de force électromotrice .
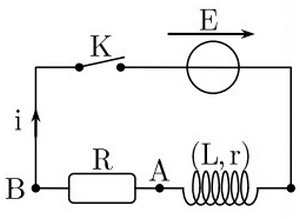
On enregistre à l’aide d’un système d’acquisition informatisé, l’intensité du courant qui traverse la bobine lorsqu’on ferme l’interrupteur .
Le résultat de l’enregistrement est donné par la courbe suivante où est la tangente à :

- Par application de la loi d’additivité des tensions, établir l’expression de l’intensité du courant en régime permanent en fonction des grandeurs , et .
- Déduire la valeur de la résistance totale du circuit .
- Montrer que l’équation différentielle vérifiée par l’intensité s’écrit sous forme .
- Déterminer l’expression de .
- Vérifier que est une solution de cette équation différentielle.
- Justifier le nom « constante de temps » donné à et déterminer graphiquement sa valeur.
- Déduire la valeur du coefficient d’induction de la bobine.
L’évolution de la tension aux bornes de la bobine ainsi que celle de la tension aux bornes du conducteur ohmique au cours du temps est donnée par le graphe suivant :
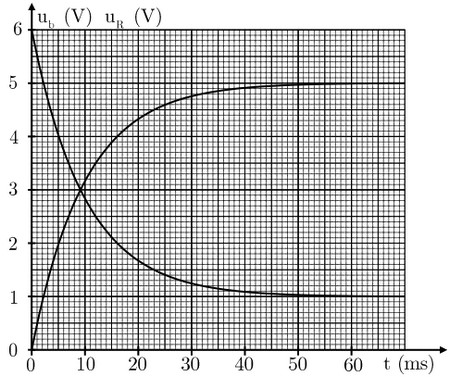
- Identifier les deux courbes.
- Déterminer les valeurs des résistances et .
Exercice 3 (7 pts)
Partie 1 : Réaction d’une base avec l’eau
On considère deux solutions basiques et de même concentration à .
- : Solution d’ammoniac de .
- : Solution de méthyle-amine de et .
- Écrire l’équation de réaction entre méthyle amine et l’eau
- Déterminer le taux d’avancement final en fonction de , et . Calculer sa valeur. Que peut-on conclure ?
- A votre avis quelle est la base la plus soluble dans l’eau ou ? justifier
- Exprimer le quotient de la réaction à l’équilibre en fonction de et . Puis calculer sa valeur.
- Quelle est l’espèce prédominante ou dans la solution ,
- Calculer le pourcentage de l’espèce prédominante.
- Déterminer la valeur de lorsque .
Partie 2 : Diagramme de réparation
Le document suivant représente le diagramme de distribution d’un mélange d’acide benzoïque , noté et d’ion benzoate noté à . il indique les pourcentages d’acide benzoïque et d’ion benzoate en solution en fonction du :
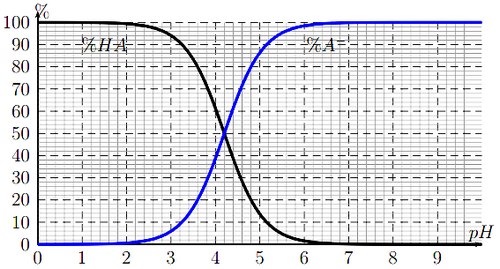
La concentration molaire totale apportée en acide et base conjugué est .
- À partir du diagramme déterminer la valeur du du couple .
- À partir du diagramme déterminer la concentration molaire en acide dans une solution de .
Données


