
Physique et Chimie : 2ème Année Collège
Séance 2 (Quelques propriétés de l’air et ses constituants)
Professeur : Mr El GOUFIFA Jihad
Sommaire
I- Introduction
II- Composition de l'air
2-1/ Expérience
2-2/ Observation
2-3/ Conclusion
III- Quelques propriétés de l'air
3-1/ Volume et pression de l'air
3-2/ Explication par le modèle particulaire
IV- Masse de l'air
4-1/ Expérience
4-2/ Observation
4-3/ Conclusion
V- Exercices
5-1/ Exercice 1
5-2/ Exercice 2
5-3/ Exercice 3
5-4/ Exercice 4
I- Introduction
L’air qui nous entoure est un mélange de plusieurs gaz.
- Quelles sont les propriétés de l’air ?
- De quoi est-il constitué?
II- Composition de l'air
2-1/ Expérience
On pose sur une bougie allumée dans un récipient pleine d'eau colorée une éprouvette graduée.

2-2/ Observation
L'eau monte dans l'éprouvette de 1/5 : elle prend la place du gaz consommé.
La bougie s'éteint : pas d'oxygène.
2-3/ Conclusion
L'air est un mélange homogène de nombreux gaz, mais ses principaux constituants sont :
- Le dioxygène (21%)
- Le diazote (78%)
- D'autres gaz (1%)
III- Quelques propriétés de l'air
3-1/ Volume et pression de l'air
Expérience
Prenons une seringue reliée à un manomètre. Comprimons l'air emprisonné dans la seringue. Tirons maintenant au contraire le piston de la seringue.
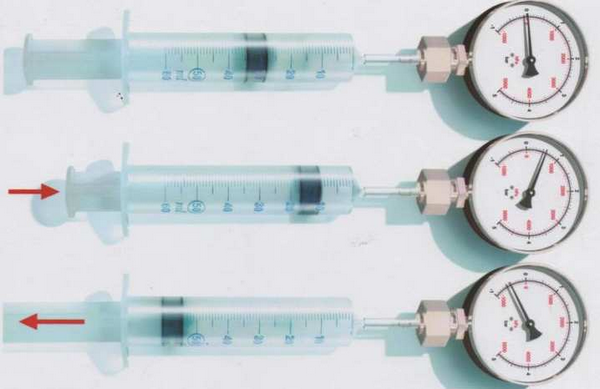
Observation
Lorsqu’on pousse le piston de la seringue, le volume de l’air diminue et sa pression augmente.
Lorsqu’on tire le piston, le volume de l’air augmente et sa pression diminue.
Conclusion
Comme tous les gaz, l’air est compressible et expansible, il n’a pas de volume propre.
III- Quelques propriétés de l'air
3-2/ Explication par le modèle particulaire
On va considérer l’air comme un ensemble de particules trop petites pour être visibles a l’œil:


- Le nombre de particules ne change pas.
- La taille et la forme des particules ne change pas.
- Quand l'air est comprimé, les particules sont moins espacées (la distance entre les particules diminue).
Conclusion
Quand l'air est comprimé, les particules sont moins espacées, le volume occupé par l'air est plus petit et donc la pression est plus grande.
C'est pourquoi une petite bouteille de plongée peut contenir plusieurs centaines de litres d'air.
IV- Masse de l'air
4-1/ Expérience
On pose un ballon bien gonflé sur le plateau de la balance et on mesure sa masse et note sa valeur
On dégonflant légèrement le ballon, on recueille 2 litre d’air du ballon par déplacement d’eau.
On pose à nouveau le ballon sur le plateau de la balance et on mesure sa masse et note sa valeur

4-2/ Observation
La masse de l'air retiré du ballon (2 litres):
4-3/ Conclusion
L'air a une masse
La masse d'un litre d'air est de 1,3 g dans les conditions habituelles (P = 1013hpa) et (θ = 25oC).
V- Exercices
5-1/ Exercice 1
Placer les mots suivants dans la bonne place :
diazote - gaz - dioxygène - 1.3 g - manomètre - pascal - mélange - dioxygène
- L’air est un ___________ constitué principalement de deux ___________
- L’air contient environ 80 % de ___________ et 20 % de ___________
- Le gaz indispensable à la vie est le ___________
- Dans les conditions normales de température et de pression, la masse d’un litre d’air est de ___________
- La pression d’un gaz se mesure avec un ___________ . L’unité de mesure de la pression est le ___________ .
V- Exercices
5-2/ Exercice 2
Amal a placé une seringue bouchée dans trois positions.

- Quelle est la position qui correspond a une compression ?
- Comparer la pression de l'air a l’intérieur de la seringue avec la pression atmosphérique dans chaque cas. Justifier
- Recopier les seringues 2 et 3 puis représenter les grains de matière.
- Choisir la bonne réponse
A- De la position 1à 2 :
- la pression diminue.
- le nombre de grains de matière diminue.
- la masse d’air enfermé augmente.
B- De la position 2 à 3 :
- le nombre de grains de matière augmente.
- le volume d’air diminue.
- la pression diminue.
V- Exercices
5-3/ Exercice 3
Amel mesure la masse d’un ballon bien gonflé. Elle lit sur la balance .
Avec une pompe, elle ajoute une certaine quantité d'air.
Elle mesure de nouveau la masse du ballon et lit .

- Quelle est la masse d’air ajouté dans le ballon ?
- Sachant que dans les conditions normales de température et de pression, la valeur de la masse de d’air est , calculer le volume d’air atmosphérique introduit dans le ballon.
V- Exercices
5-4/ Exercice 4
Un briquet contient du butane.
Pour déterminer la masse de 1.5L de gaz butane, on réalise l’expérience suivante :

- Quelle est la masse m1 du briquet avant l’extraction du butane ?
- Quelle est la masse m2 du briquet après l’extraction du butane ?
- Quelle est la masse m du butane extrait ?
- Calculer la masse volumique du butane dans les conditions ordinaires.
- Le butane est-il un gaz plus ou moins dense que l'air?


